
黒田 俊一
1.はじめに
次世代情報社会において「ヒト嗅覚情報の記録、保存、伝送、再構成(一連の流れを『匂い情報DXと定義』」を実現するには、ヒト嗅覚が感じる全ての匂いを、出来るだけ単純な共通フォーマットで客観的かつ一意的なデジタルデータとして表現する必要がある。そのために使用する匂い評価法は、限られた匂いしか検出できない酸化金属や有機ポリマーによる従来型匂いセンサ、匂わない気体分子も全て検出しデータが膨大化するGC-MS(ガスクロマトグラフ・質量分析計)、各個人の嗅覚特性に依存した主観的な官能試験などがあるが、これらは匂い情報DX実現には必ずしも適していない。それは,匂い分子だけでも40万種類以上存在し,通常は複合臭で存在するので,その組成は無数になることが大きな理由である。
一方,約1兆種類の単純臭や複合臭を識別可能なヒト嗅覚は、嗅上皮に存在する嗅神経細胞(Olfactory sensory neuron; OSN)に発現する嗅覚受容体(Olfactory receptor; OR)全て(本論文では388種類)が、それぞれ匂い対し異なる強度で応答し、全体でパターン認識する1)。そこで,各ORの応答強度を指標にすれば、ヒトが感じるほぼ全ての匂いを388次元のパラメーターで表現可能になると考えられた。
本稿では、匂い情報DXを強力に推進するために開発した全ヒトOR発現細胞(388種類)を使用したヒト嗅覚受容体センサについて紹介する。
2.ヒト嗅覚受容体センサの開発
当初は、マウス嗅上皮からOSNを単離して、任意の匂いに応答するOR群を同定する試み(deorphanization)が数多くなされてきた。最近では、マウス嗅上皮由来細胞をセルアレイ化して、匂いに応答したOSNだけを、1細胞単離するロボットが開発されているが2)、ヒト嗅上皮の単離は倫理的にも不可能であるため、全ヒトOR遺伝子を異種細胞に発現させたライブラリーから匂いに応答するOR発現細胞を探索する方法が主流である3)。
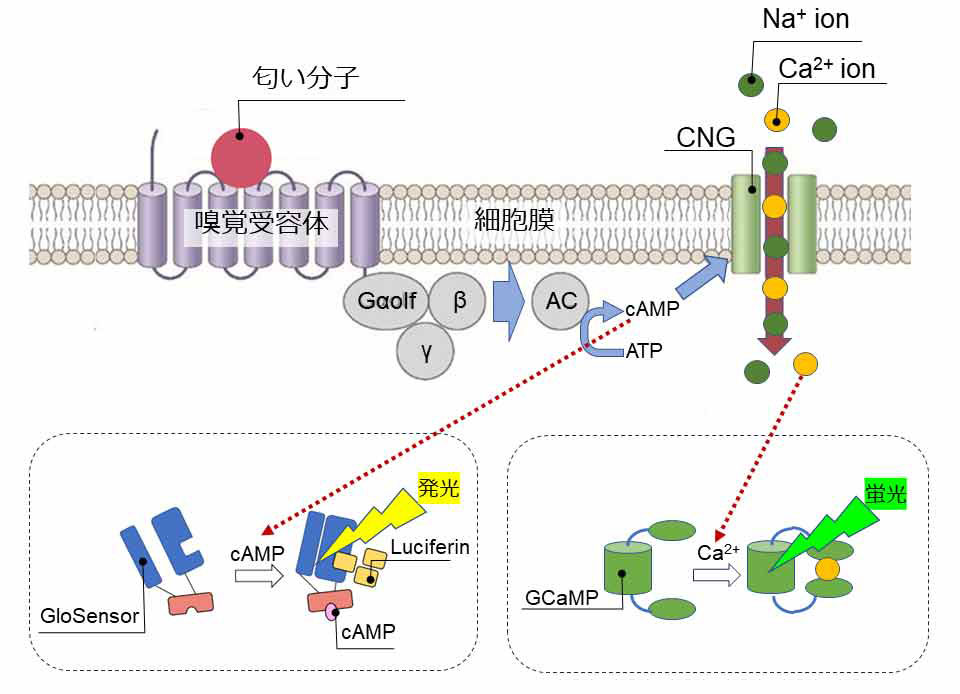
しかし、ORを異種細胞で発現すると、ORが小胞体に凝集・蓄積し分解されることが多く4)、全てのヒトORを細胞表面に提示させ、匂い分子応答可能にすることは困難であった。松波らは、シャペロンであるRTP1,RTP2,REEP1を導入したHEK293細胞(Hana3A)と、N末端にRhoタグを付加したORの組合せが,大幅に細胞表面発現を改善することを見出した5)。特にRTP1のC末端側が異なるRTP1SがORの細胞表面発現や匂い分子応答をより強く改善した6)。また、Lucyタグ7)やIL-6-Haloタグ8)が、Rhoタグよりも幅広いORの細胞表面発現を可能にした。さらに、非ORのGタンパク質共役型受容体(βAR, M3R)の共発現がORとヘテロダイマーを形成して細胞表面への移行を改善した9,10)。特に、M3Rの共発現はβアレスチン2を介するORのインタナライザーションを抑制した11,12)。次に、OSN特異的なGタンパク質α GNAL13)、Gαタンパク質のシャペロンであるRic-8B14)などの共発現、高感度なcAMP検出用LuciferaseであるGloSensorの採用15)などにより、セカンドメッセンジャー(cAMP)生成・検出系の改善も行われている(図1左下)。
以上の試みにより、大半のヒトORがHEK293細胞の細胞表層で匂い分子認識ができるようになり、任意の匂い分子に対して応答する嗅覚受容体群を同定することが可能になってきている16)。さらに最近では、全てのORを細胞表面発現させるために、RTP非依存的に細胞表面発現するORの構造的特徴が見出されている17,18)。しかし、この構造的特徴の導入は、OR本来の匂い分子認識能を変化させる可能性があり、ヒトOR全てを使用する網羅的deorphanizationには現時点では採用できない。
以上の全てのORの細胞表面発現と匂い分子応答能を改善する試みは非常に重要であるが、その多くが匂い刺激後30分間から4時間のOR応答によるセカンドメッセンジャーcAMP生成量のエンドポイント測定である。ヒト嗅覚は匂い刺激直後から強く応答し数分間のうちに順応する。この過程はOSNのOR応答に大きく依存しており、匂い情報DXを実現するためには、OSNの活動電位変化をリアルタイム測定することが最善であるが、現状では多くのOR発現細胞を一度に測定するのは困難であるので、細胞内Ca2+変化をリアルタイム測定するのが望ましい19)。
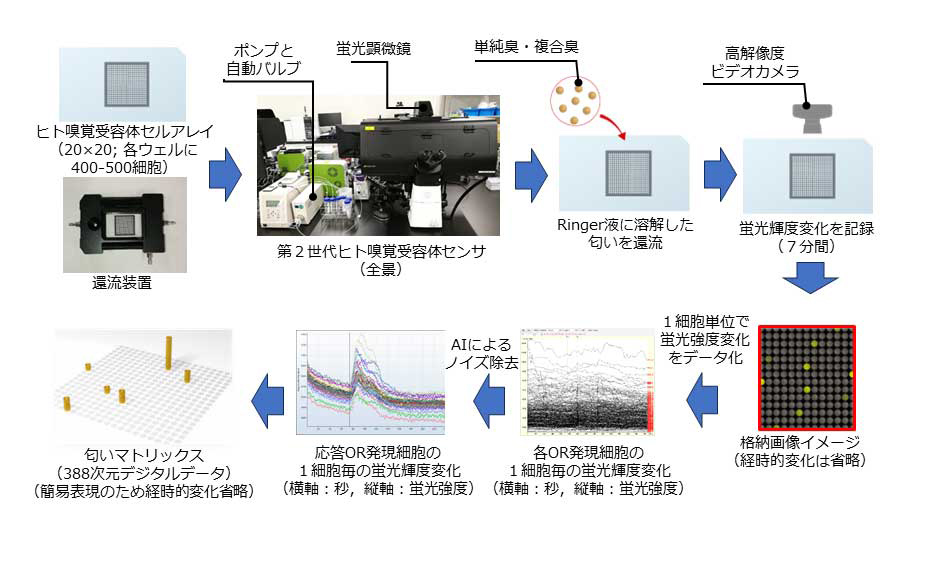
具体的には、上記OR発現細胞に、環状ヌクレオチド作動性チャネル(CNG)とCa2+依存性蛍光タンパク質(GCaMP)を導入し、388種類のヒトORをそれぞれ発現したHEK293T細胞を用意する20)(図1右下)。次に、スライドグラス上に0.5mm四角のマイクロウェルを20列×20行に配置し、ロボットを使用して、各マイクロウェルに各OR発現細胞を約400-500細胞ずつ整列配置したセルアレイとし、還流装置にセットし、蛍光顕微鏡で観察する(ヒト嗅覚受容体センサ)。対象の匂いを溶解したリンゲル溶液を還流させ、アレイ全体をビデオ撮影して、匂い分子に応答するORを発現する細胞が発する蛍光を記録する(図2上段)。
1細胞解析により得られた各細胞の膨大な波形から、機械学習したAIプログラムにより、匂いに応答したOR由来の波形を抽出し、平準化した各ORの応答波形を得る。この方法により、筆者らは数多くの匂いを388種類のヒトORの応答強度で、単純臭、複合臭を問わず表現できる(匂いマトリックスと呼ぶ)(図2下段)。この時、同じORでも異なる匂い分子に対する応答波形は異なるので、この匂いマトリックスは各ORにつきそれぞれ経時的変化も含んでいるが、通常は簡略化のためスナップショットを使用している20)。このセルアレイ技術に基づくヒト嗅覚受容体センサは、製薬会社においてGPCR作動薬のスクリーニングに使用されている多くのマイクロプレートと試薬を必要とするFLIPR21)よりも、遥かに迅速かつ安価に、しかも同じ測定セットで異なる条件を連続して測定できる。
3.ヒト嗅覚受容体センサによる匂い情報DX
ヒト嗅覚において全ORがどのように匂いを認識しているかを正確に調べる網羅的deorphanizationを行うには、現行のヒトOR発現細胞では課題が多い。まず、発現に使用している細胞に含まれるGαタンパク質がOSNと異なる場合、ORの匂い分子応答が変化する22)。また、ヒトORには点突然変異(SNPs)が数多く見られ匂い分子応答が変化する23-25)。さらに、液相中の匂いに対するOR応答を測定しており、ヒト嗅覚では気相中の匂いを、鼻汁を介してOSNのORが応答するので検出感度に大きな差が生じる。しかしながら、匂い情報DXの実現(特に、記録)のためには、固定されたヒトORセットにより、一定の条件で匂いを測定し、ヒトが感じる匂いを全て388次元の匂いマトリックスで定義できれば十分であり、ヒト嗅覚による匂いの感じ方を正確に反映する必要はない。
これまで、任意の匂いを再構成するには、オリジナルの匂いをGC-MSで成分分析して、主要香気成分を同じ割合で混合すれば再構成できた。しかし、それでは約40万種類と言われる匂い分子全てを用意しなければ、匂い情報DXの再構成を実現できず、実質的に不可能である。特定の香料群(アロマ精油)をGC-MS分析して、同じ香調を示す匂い分子を整理して、任意のアロマ精油の香調を再現する試みがあるが、この方法は広範囲な匂いの再構成には使用できない26)。
筆者らはヒト嗅覚受容体センサとGC-MSを用いて、鰹節、バラ精油、ラベンダー精油、バニラ香料の香気成分を測定した。その結果、各サンプルは数多くの気体成分を含んでいるにもかかわらず、顕著に応答したヒトORは10種類以下であった。また応答ORの中には共通したものが含まれており、鰹節に応答した10種類のORのうち、4種類がバニラ香料にも応答した。バラ精油に4種類のORのうち、1種類がラベンダー精油にも応答した。さらに、各ORをピンポイントに刺激する匂い分子をサンプルには含まれていない匂い分子から選抜し、匂いマトリックスを再現できる比率で混合したところ、鰹節は7種類、バラ精油は4種類、ラベンダー精油は3種類、バニラ香料は5種類のサンプルには含まれていない匂い分子で、オリジナルのサンプルとほぼ同じ香調を示すことができた(㈱香味醗酵HP掲載データ)。この結果は、どんなに複雑な匂いでも、ヒト嗅覚受容体センサにより匂いマトリックスを得て、各応答ORをピンポイントで刺激する匂い分子を混合すれば、遥かに少ない種類の匂い分子で再現可能であることを示している27)。
これまでに、複合臭に対するOSNの応答は、各匂い成分のOSN応答と基本的に線形であるが28)、匂い分子同士の干渉が存在し29)、非線形なOR応答が時折観察される30)。また、濃度依存的に同じ匂い分子がOR応答を促進したり抑制したりするInverse agonistが存在する31)。これらの複合臭における例外的な匂い分子の作用は予期せず起きるため,従来の匂いセンサやGC-MSで匂いを測定しても正確な香調の評価が困難である。
以上から,特に複合臭に対する香調評価にはヒト嗅覚受容体センサのみが有効であり、匂い情報DX実現に必要な,任意の匂いと同じ香調を有する匂いの再構成に使用する匂い分子は、各ORをピンポイントで刺激する匂い分子のみを使用するほうがよい。
次回に続く-
参考文献
- Malnic B, Hirono J, Sato T, Buck LB 1999 Combinatorial receptor codes for odors. Cell 96 713-23.
- Suzuki M, Yoshimoto N, Shimono K, Kuroda S. 2016 Deciphering the receptor repertoire encoding specific odorants by time-lapse single-cell array cytometry. Sci. Rep. 6 19934.
- Peterlin Z, Firestein S, Rogers ME. 2014 The state of the art of odorant receptor deorphanization: a report from the orphanage. J. Gen. Physiol. 143 527-542.
- Lu M, Echeverri F, Moyer BD. 2003 Endoplasmic reticulum retention, degradation, and aggregation of olfactory G-protein coupled receptors. Traffic 4 416-33.
- Saito H, Kubota M, Roberts RW, Chi Q, Matsunami H. 2004 RTP family members induce functional expression of mammalian odorant receptors. Cell 119 679-691.
- Wu L, Pan Y, Chen GQ, Matsunami H, Zhuang H. 2012 Receptor-transporting protein 1 short (RTP1S) mediates translocation and activation of odorant receptors by acting through multiple steps. J. Biol. Chem. 287 22287-22294.
- Shepard BD, Natarajan N, Protzko RJ, Acres OW, Pluznick JL. 2013 A cleavable N-terminal signal peptide promotes widespread olfactory receptor surface expression in HEK293T cells. PLoS One 8 e68758.
- Noe F, Frey T, Fiedler J, Geithe C, Nowak B, Krautwurst D. 2017 IL-6-HaloTag® enables live-cell plasma membrane staining, flow cytometry, functional expression, and de-orphaning of recombinant odorant receptors. J. Biol. Methods. 4 e81.
- Hague C, Uberti MA, Chen Z, Bush CF, Jones SV, Ressler KJ, Hall RA, Minneman KP. 2004 Olfactory receptor surface expression is driven by association with the beta2-adrenergic receptor. Proc. Natl. Acad. Sci. USA. 101 13672-13676.
- Li YR, Matsunami H. 2011 Activation state of the M3 muscarinic acetylcholine receptor modulates mammalian odorant receptor signaling. Sci. Signal. 4 ra1.
- Mashukova A, Spehr M, Hatt H, Neuhaus EM. 2006 Beta-arrestin2-mediated internalization of mammalian odorant receptors. J. Neurosci. 26 9902-9912.
- Jiang Y, Li YR, Tian H, Ma M, Matsunami H. 2015 Muscarinic acetylcholine receptor M3 modulates odorant receptor activity via inhibition of β-arrestin-2 recruitment. Nat. Commun. 6 6448.
- Jones DT, Reed RR. 1989 Golf: an olfactory neuron specific-G protein involved in odorant signal transduction. Science 244 790-795.
- Papasergi MM, Patel BR, Tall GG. 2015 The G protein α chaperone Ric-8 as a potential therapeutic target. Mol. Pharmacol. 87 52-63.
- Kida H, Fukutani Y, Mainland JD, de March CA, Vihani A, Li YR, Chi Q, Toyama A, Liu L, Kameda M, Yohda M, Matsunami H. 2018 Vapor detection and discrimination with a panel of odorant receptors. Nat. Commun. 9 4556.
- Saito H, Chi Q, Zhuang H, Matsunami H, Mainland JD. 2009 Odor coding by a mammalian receptor repertoire. Sci. Signal. 2 ra9.
- Ikegami K, de March CA, Nagai MH, Ghosh S, Do M, Sharma R, Bruguera ES, Lu YE, Fukutani Y, Vaidehi N, Yohda M, Matsunami H. 2020 Structural instability and divergence from conserved residues underlie intracellular retention of mammalian odorant receptors. Proc. Natl. Acad. Sci. USA 117 2957-2967.
- Fukutani Y, Nakamura Y, Muto N, Miyanaga S, Kanemaki R, Ikegami K, Noguchi K, Ohsawa I, Matsunami H, Yohda M. 2021 Hot spot mutagenesis improves the functional expression of unique mammalian odorant receptors. Int. J. Mol. Sci. 23 277.
- Menini A. 1999 Calcium signaling and regulation in olfactory neurons. Curr. Opin. Neurobiol. 9 419-426.
- Yasunaga M, Takai E, Hattori S, Tatematsu K, Kuroda S. 2022 Effects of 3-octen-2-one on human olfactory receptor responses to vanilla flavor. Biosci. Biotechnol. Biochem. 86 1562-1569.
- Emkey R & Rankl NB 2009 Screening G protein-coupled receptors: Measurement of intracellular calcium using the fluorometric imaging plate reader. Methods Mol. Biol. 565 145-158.
- Shirokova E, Schmiedeberg K, Bedner P, Niessen H, Willecke K, Raguse JD, Meyerhof W, Krautwurst D. 2005 Identification of specific ligands for orphan olfactory receptors. G protein-dependent agonism and antagonism of odorants. J. Biol. Chem. 280 11807-11815.
- Mainland JD, Keller A, Li YR, Zhou T, Trimmer C, Snyder LL, Moberly AH, Adipietro KA, Liu WL, Zhuang H, Zhan S, Lee SS, Lin A, Matsunami H. 2013 The missense of smell: functional variability in the human odorant receptor repertoire. Nat. Neurosci. 17 114-120.
- Jaeger SR, McRae JF, Bava CM, Beresford MK, Hunter D, Jia Y, Chheang SL, Jin D, Peng M, Gamble JC, Atkinson KR, Axten LG, Paisley AG, Tooman L, Pineau B, Rouse SA, Newcomb RD. A 2013 Mendelian trait for olfactory sensitivity affects odor experience and food selection. Curr. Biol. 23 1601-1605.
- Trimmer C, Keller A, Murphy NR, Snyder LL, Willer JR, Nagai MH, Katsanis N, Vosshall LB, Matsunami H, Mainland JD. 2019 Genetic variation across the human olfactory receptor repertoire alters odor perception. Proc. Natl. Acad. Sci. USA. 116 9475-9480.
- Debnath T, Nakamoto T. 2022 Extraction of sensing data for desired scent impressions using mass spectra of odorant molecules. Sci. Rep. 12 16297.
- Kuroda S, Nakaya-Kishi Y, Tatematsu K, Hinuma S. 2023 Human olfactory receptor sensor for odor reconstitution. Sensors (Basel). 23 6164.
- Gupta P, Albeanu DF, Bhalla US. 2015 Olfactory bulb coding of odors, mixtures and sniffs is a linear sum of odor time profiles. Nat. Neurosci. 18 272-281.
- Reddy G, Zak JD, Vergassola M, Murthy VN. 2018 Antagonism in olfactory receptor neurons and its implications for the perception of odor mixtures. Elife. 7 e34958.
- Singh V, Murphy NR, Balasubramanian V, Mainland JD. 2019 Competitive binding predicts nonlinear responses of olfactory receptors to complex mixtures. Proc. Natl. Acad. Sci. USA. 116 9598-9603.
- Inagaki S, Iwata R, Iwamoto M, Imai T. 2020 Widespread inhibition, antagonism, and synergy in mouse olfactory sensory neurons in vivo. Cell Rep. 31 107814.
【著者紹介】
黒田 俊一(くろだ しゅんいち)
大阪大学 産業科学研究所 所長/教授
■略歴
1984年 京都大学農学部農芸化学科卒業
1986年 京都大学大学院農学研究科修士課程修了(農芸化学専攻)
同年 武田薬品工業(株)生物工学研究所研究員
1992年 京都大学博士(農学)
1994年 神戸大学バイオシグナル研究センター助手
1996年 同助教授
1998年 大阪大学産業科学研究所助教授
2002年 ジュネーブ大学医学部客員教授(兼任)
~03年
2009年 名古屋大学大学院生命農学研究科教授
2015年 大阪大学産業科学研究所教授
2017年 (株)香味醗酵取締役(最高科学担当)
~23年
2024年 大阪大学産業科学研究所所長
現在に至る
製薬会社において遺伝子組換えタンパク質製剤の開発研究,大学では細胞内情報伝達機構の研究,DDSナノキャリア開発,全自動1細胞解析単離装置の開発を行った後,現在はヒト嗅覚受容体発現細胞セルアレイセンサの開発と社会実装を行う。日本農芸化学会奨励賞,同学会技術賞,バイオビジネスコンペJAPAN優秀賞,日本バイオベンチャー大賞文部科学大臣賞,ものづくり日本大賞(経済産業大臣賞)などを受賞。
