
ポストLEDフォトニクス研究所
特任助教
加藤 遼
3.
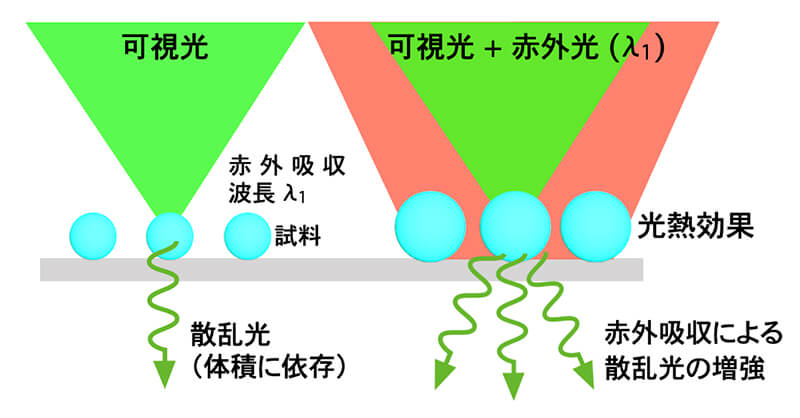
そこで、我々のグループでは、中赤外吸収の高い検出感度を保ちつつ、可視光の高い空間分解能で分子振動情報を可視化することができる超解像中赤外分光顕微鏡の開発に取り組んできた。この顕微鏡では、中赤外吸収に伴う光熱変換を利用して、分子の中赤外吸収を検出する。ある赤外光の波長で吸収を示す分子にその波長の中赤外光を照射すると、吸収されたエネルギーは試料内部で熱に変換される。この熱による分子内部の温度変化は、試料の屈折率変化や体積膨張を引き起こす。この手法では、赤外光に加えて可視光も同時に試料に照射し、その散乱光や反射光を検出する。可視光の反射光や散乱光の強度や進行方向は、Mie理論に基づいて試料の屈折率や体積に依存するため、光熱変換による屈折率変化や体積膨張が可視光の光学応答も変調する。従って、可視光の光学応答を計測することで、間接的に分子の赤外吸収を測定することができる(図2)。検出する赤外吸収情報は可視光が照射される領域の情報である。つまり、可視光の空間分解能で赤外吸収情報を可視化することができる。また、この手法では赤外光は試料に当たりさえすれば良いので、中赤外光が試料を透過する際に吸収され測定が困難になる懸念もない。
4.
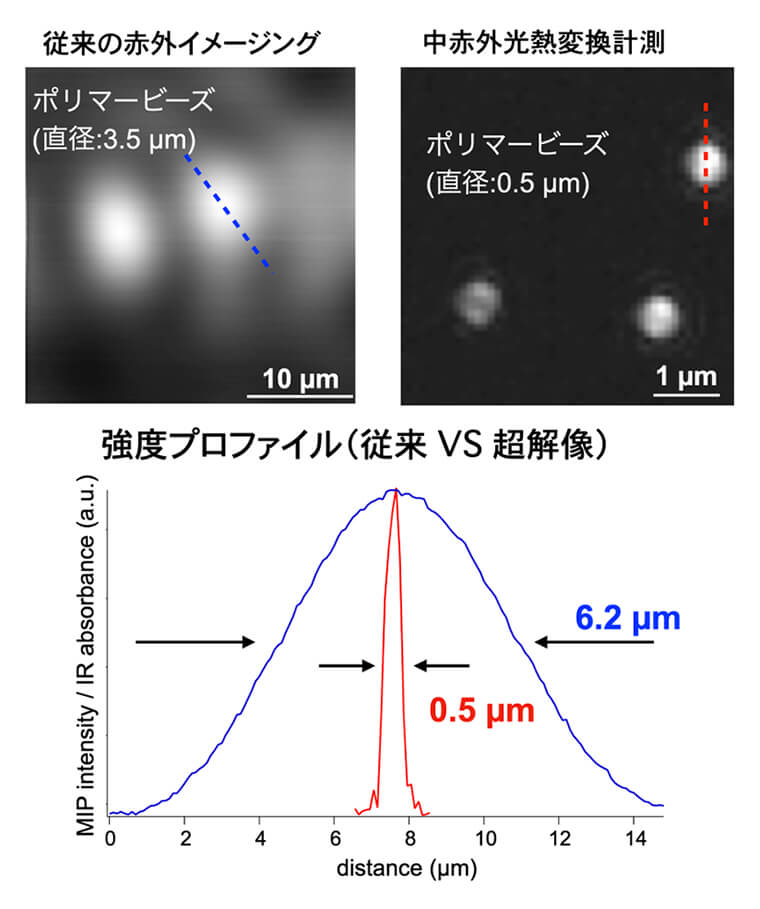
図3に、中赤外光熱変換計測の簡略化された光学系を示す。実際には、可視の連続光と中赤外のパルス光を試料に照射する。赤外パルス光によって瞬間的な体積膨張が引き起こされ、その際の可視光の散乱光や反射光の強度変化を検出する。我々のグループを含め、国内外で数グループが中赤外光熱変換計測を独自開発してきた。中赤外光熱変換計測の最大の利点は、サブミクロンの空間分解能を持つことである。図4に示すのは、従来の赤外顕微鏡で撮像されたポリマー粒子(直径3.5 µm)の赤外吸収像と、我々が開発した中赤外光熱変換顕微鏡で取得したポリマー粒子(直径0.5 µm)の赤外強度像である。どちらもポリスチレンの赤外吸収強度(波数1494 cm-1)で画像化されたものである。中赤外光熱変換顕微鏡では、サブミクロンの直径を持つ対象物であっても可視化できることが示されている。また、強度のラインプロファイルからも空間分解能の向上が明らかであり、従来と比較して10倍以上も高い空間分解能が得られている。近年では、非線形光学効果を利用した光熱変換計測により、200 nmの空間分解能での可視化も報告されている。
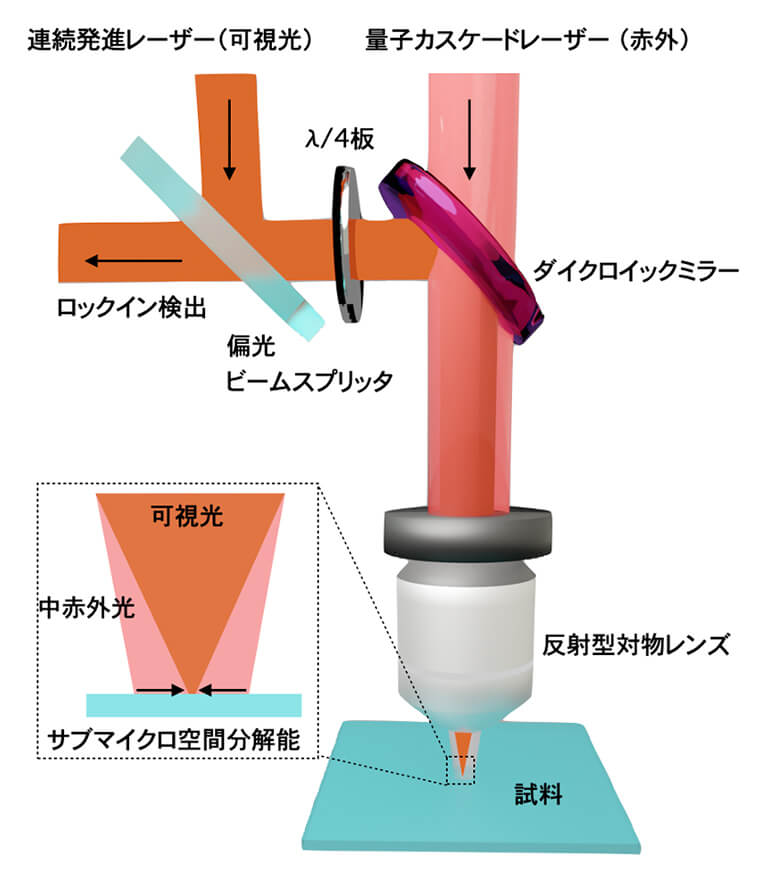
中赤外光熱変換顕微鏡の一般的な装置構成は、可視光と中赤外光を同軸で反射型対物レンズによって集光し、反射光や透過光の強度をロックイン検出法で計測する方法である(図3)。この手法の最大の利点は、観察対象の制約がないことである。つまり、不透明な試料や大きなサイズの試料であっても観察できる。実際に、我々もこの正立型の中赤外光熱変換計測装置を開発し、厚みのある生体組織や錠剤、歯科材料の組成分析を行ってきた。一方で、可視光と中赤外光を別々の対物レンズで反対方向から集光する光学系も開発されている。この手法の利点は、可視光を高い開口数を持つ回折型対物レンズで集光できるため、高感度かつ高空間分解能が得られる点である[2]。実際にこの構成を用いた研究では、我々は厚さ7 nmのポリマー膜の検出に成功している。他のグループも100 nmのポリマー粒子やウイルス粒子を可視化した例を報告している。また、他の光学技術との統合、たとえばラマン分光や蛍光分光などとの組み合わせも容易であり、マルチモーダルな生体分析の報告例もある。上記は、可視光と赤外光を集光しステージを走査して画像を取得する機構であるが、デジタルホログラフィーやLEDを用いたワイドフィールド型の中赤外光熱変換計測イメージングの報告例もある。ワイドフィールド型は、時間分解能を向上させることができるが、照明ムラによる定量性の低下や、集光型に比べて感度が低く赤外吸収の利点を損なう点など、一長一短である。
5.
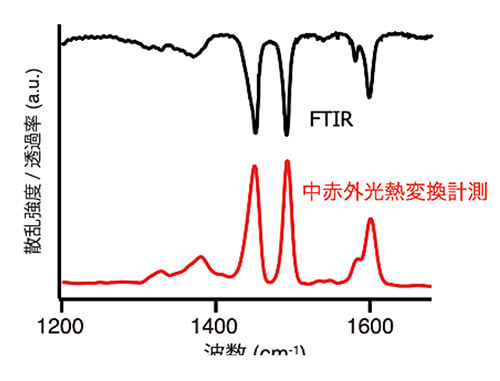
中赤外光熱変換計測においては、分子の赤外吸収スペクトルを再現できるかという点について議論がある。図5に示すのは、従来のフーリエ変換赤外分光法(FTIR)と、我々が開発した装置で取得したポリスチレンの赤外スペクトルである。中赤外光熱変換計測では、照射する赤外パルス光の波数を変化させながら可視光の応答を計測し、赤外スペクトルを得ることができる。ポリスチレンのFTIRスペクトルと中赤外光熱変換スペクトルの形状やスペクトル特性は一致していることが分かる。スペクトル形状のわずかな違いは、光熱変換計測では量子カスケードレーザーを赤外光源として使用しているため、偏光特性がスペクトルに反映されているものと考えられる。
中赤外光熱変換顕微鏡を用いた生体イメージングは、我々を含め国内外の研究グループによって精力的に行われている。特に、Minhaeng Choらのグループでは、中赤外光熱変換顕微鏡を用いて希突起膠細胞のタンパク質分布を可視化することで、細胞分裂の様子を経過観察できており、生物学的に重要な応用例を示している。Ji-Xing Chengらのグループは、中赤外光熱変換顕微鏡を用いた大腸菌の代謝イメージングを行い、複数の薬剤耐性を観察している。これは、微生物学的に極めて重要な可視化研究であると我々は位置付けている。
我々も生体組織内の分子をラベルフリーで可視化することに成功し、医学応用へのポテンシャルを示した[3]。
6.
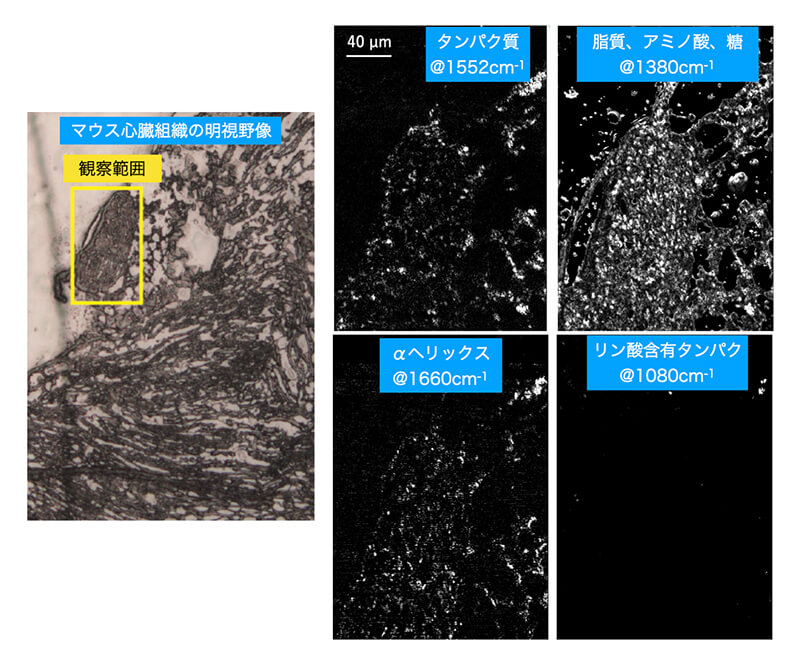
図6はマウスの心臓組織の中赤外光熱変換イメージング結果である。生体組織の中赤外光熱変換スペクトルには複数の特徴的なピークが現れ、それぞれが異なる分子に特有のピークである。各分子に特有の赤外信号の波数における強度で画像化することで、タンパク質、脂質、アミノ酸、糖の分布を可視化できる。また、赤外分光は分子の化学構造や官能基に関する情報も観察できるため、例えばαヘリックス構造を持つタンパク質やリン酸化したタンパク質など、特定のタンパク質の二次構造やリン酸化も可視化できる。特に、タンパク質の二次構造やリン酸化は疾患の指標となることがあり、これらの生体分子の物性を可視化することの医学的な意義は極めて大きいと考える。また、我々は血球細胞内のタンパク質物性を1細胞レベルで解析し、細胞ごとの組成の不均一性を観察することにも成功している。近年は微生物内の分子物性やそれらが引き起こす物理現象の可視化も行っている。例えば、シアノバクテリアが生産する細胞外多糖が形成するバイオフィルムや細胞の自己集合、糸状菌の細胞壁や脂肪滴の化学組成などの可視化に注力している。生体イメージングだけでなく、材料科学分野への応用も精力的に行われている。Hartlandらはペロブスカイト薄膜の分子組成の不均一性と電子エネルギー特性を中赤外光熱変換顕微鏡によって可視化している。我々もポリマー材料の相分離構造や有機薄膜の光反応物の可視化に成功し、材料科学分野における本技術の有効性を示してきた[4]。他の海外の研究グループでは、絵画の品質評価や哺乳瓶に付着するマイクロプラスチック、大気中のエアロゾル内の物理・化学特性など、基礎科学だけでなく実社会の改善に貢献する応用例も実証している。
7.
本稿では、サブミクロンの空間分解能と高い赤外吸収の検出効率を併せ持つ中赤外光熱変換に関する原理とその応用について紹介した。特に、生命科学や医学、材料科学分野においては、中赤外光熱変換計測の有効性がこれまで実証されてきた。近年のレーザー技術やデータ処理技術は目覚ましく進化しており、最新鋭の光学・数理学技術を活用した先端分光可視化技術は今後も増加することが予想される。
参考文献
- R. Kato, T. Yano, T. Tanaka, Analyst, 148, 1285-1290 (2023)
- R. Kato, T. Yano, T. Minamikawa, T. Tanaka, Analytical Sciences, 38, 1497–1503 (2022)
- R. Kato, T. Yano, T. Tanaka, Vibrational Spectroscopy, 118, 203333 (2022)
【著者紹介】
加藤 遼(かとう りょう)
徳島大学 ポストLEDフォトニクス研究所 特任助教
■略歴
- 2021年4月 – 2022年5月徳島大学ポストLEDフォトニクス研究所 特任研究員
- 2022年6月 – 現在徳島大学ポストLEDフォトニクス研究所 特任助教
- 2021年6月 – 現在理化学研究所 メタマテリアルグループ 客員研究員
- 2021年10月 – 現在JST ACT-X研究者「環境とバイオテクノロジー」

