
所長代理
立石 典生
1.はじめに
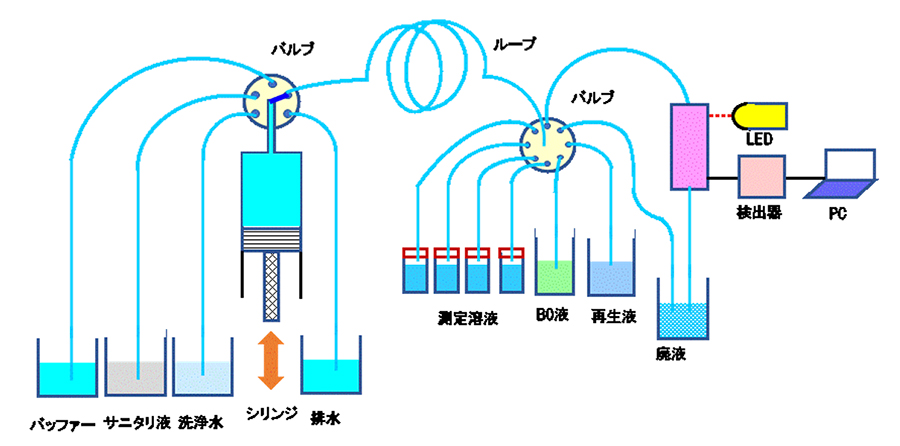
 図1 フロー式イムノセンサ
図1 フロー式イムノセンサ
このフロー式イムノセンサの構造と機能、とりわけ抗原・抗体反応を利用した検体(抗原)相当量の測定方法の原理、環境汚染物質ダイオキシン類の測定、生体の炎症反応物質の一つであるC-reactive protein (CRP)の測定、さらには小型化イムノセンサの開発について紹介する。
2.フロー式イムノセンサの構造と機能
フロー式イムノセンサは、測定溶液をシリンジポンプでセル(カラム)へ送液し、次の測定溶液を測定する場合も同様の経路を送液することになり、コンタミネーションの低減が課題となる。とりわけ、シリンジポンプ経路内のデッドボリュームに試料・試薬等が残存するため、次の測定溶液を測定する際にコンタミネーションの原因となる。そこで、図2に示すように、直接シリンジ内に試料・試薬等を吸引しないフロー系を構築することにより、送液経路内のデッドボリュームを低減したことにより、試料・試薬などの残留量を低減することで繰り返し測定の精度の向上を図った3)。本編では、このフロー式イムノセンサの構造と機能の説明・解説、並びに、小型化イムノセンサの開発・改良について紹介する。
3.フロー式イムノセンサによる測定
フロー式イムノセンサは、抗原・抗体反応に基づく免疫測定を自動化して、競合方法並びにサンドイッチ方法によって、対象物質(検体・抗原)をそれに対する特異抗体と蛍光標識2次抗体を用いて短時間で高精度に定量できる。そこで、競合方法並びにサンドイッチ方法によるフロー式イムノセンサの測定原理と各々の定量測定について例示する。
3.1 競合方法
特定の標的物質(抗原)に対して抗体認識部位(エピトープ)の異なる2種類の特異抗体の「マッチドペア」がない低分子量化合物などの測定の場合、競合方法を用いる。
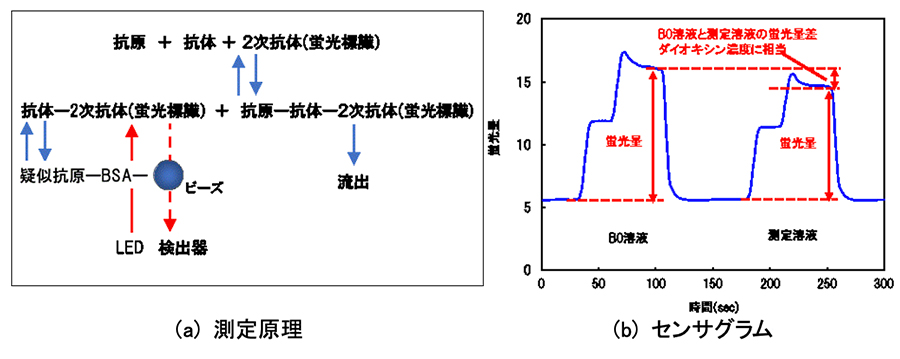
フロー式イムノセンサを用いた競合方法では、例えば、測定対象物(検体)がダイオキシン(2,3,7,8-テトラクロロジベンゾジオキシンの分子量322)の場合、ダイオキシン(検体・抗原)、抗ダイオキシン抗体(ダイオキシンハプテン抗体)及び蛍光標識2次抗体(IgG結合抗体)を混合した測定溶液には図3 (a)に示すように抗原に未反応の抗ダイオキシン抗体・蛍光標識2次抗体複合体、及び、抗ダイオキシン抗体・ダイオキシン(抗原)・蛍光標識2次抗体複合体が平衡して共存する。この溶液をセル(カラム)へ送液すると、セルにはあらかじめ疑似抗原・BSA(牛血清アルブミン)結合体を固定化したビーズが充填してあり、抗原に未反応の抗ダイオキシン抗体・蛍光標識2次抗体複合体は疑似抗原・BSA結合体に反応してビーズに捕捉される。
それに対して、抗ダイオキシン抗体・ダイオキシン・蛍光標識2次抗体複合体はカラムから流出する。セル内のビーズ表面に捕捉された蛍光標識(例えばCyanine 5またはAlexa Fluor 647) 2次抗体を励起波長650nmに対する蛍光波長665nmの蛍光強度を計測することにより蛍光量として抗原と未反応の抗ダイオキシン抗体量を定量する(図3 (b))。そのデータからダイオキシン濃度を求める4),5),6)。
即ち、ダイオキシン濃度は、セル内ビーズに捕捉された抗原未反応の抗ダイオキシン抗体の測定量ではなく、ダイオキシンと反応した抗ダイオキシン抗体の量に相当するため、図3 (b) のセンサグラムのように、ダイオキシン(検体)を含まない抗ダイオキシン抗体・蛍光標識2次抗体複合体のみのB0溶液の蛍光量を測定し、その後、ダイオキシン(検体)含有試料、抗ダイオキシン抗体及び蛍光標識2次抗体を混合した測定溶液を測定する。ビーズに補足されたB0溶液の蛍光量とダイオキシンを含む測定溶液の蛍光量の差を抗原・抗体複合体の量、すなわち、ダイオキシン相当量として定量する。
ただし、この方法は測定対象物ダイオキシンの分子量が低く毒性が高い等、取り扱いに規制のある化合物の場合、直接その化合物をセルのビーズに固定化することは困難であるため、抗ダイオキシン抗体が反応する疑似抗原・BSA結合体を使用する。また、抗ダイオキシン抗体のダイオキシン(抗原)と疑似抗原・BSA結合体に対する親和性の差が測定感度に大きく影響する。
次回に続く-
参考文献
- Lei Xie, R Mark Jones, Thomas R Glass, Ryman Navoa, Yan Wang, Michael J Grace, “Measurement of the functional affinity constant of a monoclonal antibody for cell surface receptors using kinetic exclusion fluorescence immunoassay,” J Immunol Methods, 304 (1-2), 1-14 (2005)
- Palaniswami Rathanaswami, John Babcook, Michael Gallo, “High-affinity binding measurements of antibodies to cell-surface-expressed antigens,” Anal Biochem, 373, 52-60 (2008)
- Takashi Matsuki, Eigen Nakama, Jun Kishino, Yoshinori Tokuda, Yoko Takagi, Chiwa Kataoka, Noriaki Hamada, Hiroyuki Fujita, Norio Tateishi, Kazuyuki Sawadaishi, Katsuhisa Honda, “A Simplified Dioxin Analysis System – Automatic Sample Preparation Devise and Dioxin Biosensor,” Organohalogen Compoundds, 67, 39-41 (2005)
- Robert C. Blake II, Andrey R. Pavlov, Diane A. Blake, “Automated kinetic exclusion assays to quantify protein binding interactions in homogeneous solution,” Analytical Biochemistry, 272, 123-134 (1999)
- Diane A Blake, R. Mark Jones, Robert C Blake II, Andrey R Pavlov Ibrahim A Darwish, Haini Yu, “Antibody-based sensors for heavy metal ions,” Biosens Bioelectron 16, 799-809 (2001)
- Thomas R Glass, Naoya Ohmura, Hiroshi Saiki, “Least detectable concentration and dynamic range of three immunoassay systems using the same antibody,” Anal. Chem., 79 (5), 1954-1960 (2007)
【著者紹介】
立石 典生(たていし のりお)
株式会社シーズテック 京都バイオ研究所 所長代理
■略歴
2003年 京都電子工業株式会社 入社
2004年 愛媛大学農学部環境分析化学(京都電子)講座 助手兼任(2007年3月まで)
2017年 株式会社シーズテック 入社(~現在に至る)
