
NTT先端集積デバイス研究所
味戸 克裕
3.テラヘルツ分光センシングシステム
THz分光センシングシステムは、分光のやり方によって連続波型とパルス波型とに大別することができるが、得られる情報は複素誘電率の実部と虚部、すなわち位相と吸収の度合いである。連続波型はTHz波の周波数を変えて、位相や吸収を測定するので理解はしやすいが、THz波の周波数可変の光源はTHzギャップといわれている周波数領域にあり、フォトニクス技術でもエレクトロニクス技術でも難しいため、連続波型のセンシングシステムの構築が難しい。そのため、分光の主流はパルス波型というフェムト秒レーザーを用いた特殊なシステムとなる[10]。
図5には連続波型のTHz分光センシングシステムの構成図を示す。この手法は、THz周波数領域分光 (THz-FDS: Terahertz Frequency-Domain Spectroscopy)とよばれる。
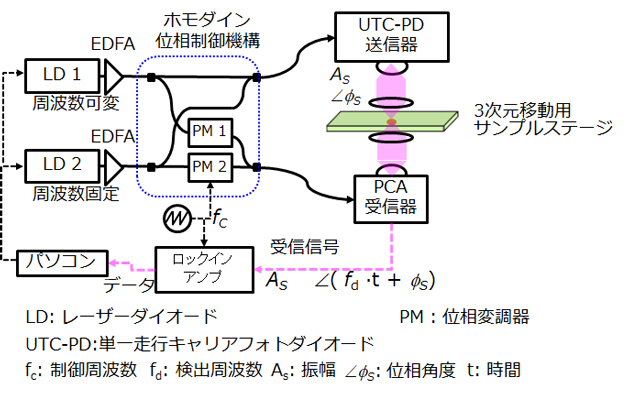
周波数可変の1.5μm帯の連続波近赤外レーザダイオードと周波数固定のもう1台のレーザダイオードをそれぞれエルビウム添加ファイバ増幅器(EDFA)で増幅し、差周波混合でフォトダイオードを使って光電変換を行い、任意の周波数のTHz波を発生させる。2台のレーザダイオードの周波数の差が発生するTHz波の周波数となる。このTHz分光センシングシステムではInPを使った高効率のTHz光発生用のフォトダイオード、単一走行キャリアフォトダイオード(UTC-PD: Uni-Traveling Carrier Photodiode)を使用している。周波数可変のレーザダイオードの周波数を変えることで0.2~2.0 THzの任意の周波数のTHz光得ることができ、周波数やアンテナ形状によって出力は変わるが、0.3 THzの周波数において最大で1mW出力を確認している[11]。UTC-PDからのTHz波を単に受信するだけでなく、位相制御機構を通して受信機のPCAに送信信号と同じ信号を入れてミキシングをすることをホモダイン検波方式と呼ぶ。ホモダイン検波方式のようなコヒーレント検出法は、位相制御機構を使わないで振幅(吸収の度合いに対応)のみを検出する一般的なエンベロープ検出法に比べてダイナミックレンジが大きくなるため、材料の吸収を測定する際に有利になる。また、複素誘電率の実部と虚部、すなわち位相と吸収の度合いに対応する値を得ることができ、材料評価に役立つ。さらに、周波数を連続的に変えることでスペクトル測定が可能であり、周波数を任意の吸収ピークに固定してステージを平面内で走査することで、高速で物質同定のイメージを取得できることがメリットである[12]。1THzは波長0.3mmに相当するので、波長の2分の1を回折限界と考えれば0.15mmの空間分解能となるが、周波数が10倍の0.1THzとなれば、1.5mmと空間分解能は低下することに注意する。
図6はパルス波型のTHz分光センシングシステムの構成図を示すが、このシステムはTHz時間領域分光 (THz-TDS: Terahertz Time-Domain Spectroscopy)システムとよばれ、1989年にIBMのGrischkowskyらが最初に水蒸気のTHzスペクトルを報告したのが最初である[13]。
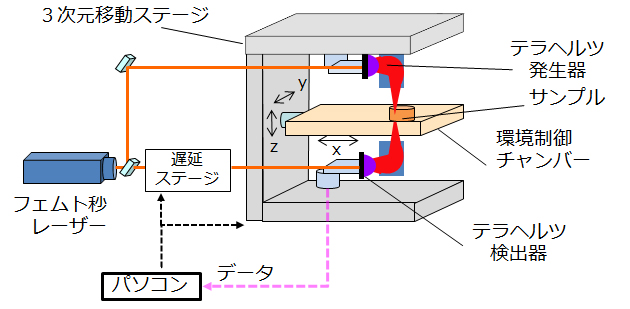
パルス幅が10~100フェムト秒の近赤外フェムト秒レーザで光伝導アンテナ(PCA: Photoconductive Antenna)を励起して、キャリアの超高速移動によってTHzパルスを発生させ、検出も同様の構成の光伝導アンテナを用い、遅延ステージを使って時間分解スペクトルを測定する。そして、得られた時間領域スペクトルをフーリエ変換することで周波数スペクトルを得る。10フェムト秒の近赤外フェムト秒レーザと低温成長GaAs膜の組み合わせの場合で約0.1~7THzの周波帯のTHzスペクトルを得ることができる[14]。さらに、3次元移動ステージを用いてサンプルを平面内で走査することでサンプルに照射するTHz光のスポット位置を移動させることができ、分光イメージングが可能であることは THz-FDSと同様である。THz-TDSの測定時間は、主に遅延ステージが律速となっているため、高速の遅延ステージほど測定時間は短くとなる。現在では1スペクトルを1ミリ秒程度で取得できるタイプも市販されており、イメージ測定もより高速となっている[15]。
4.医薬成分のテラヘルツセンシングとデータサイエンス
連続波型THzイメージングシステムを使った医薬品の共結晶の識別の例を図7に示す[16]。共結晶(コクリスタルともいう)は薬品分野において注目されている複合分子結晶で、API結晶と各種の添加剤結晶から成る複合分子結晶である。
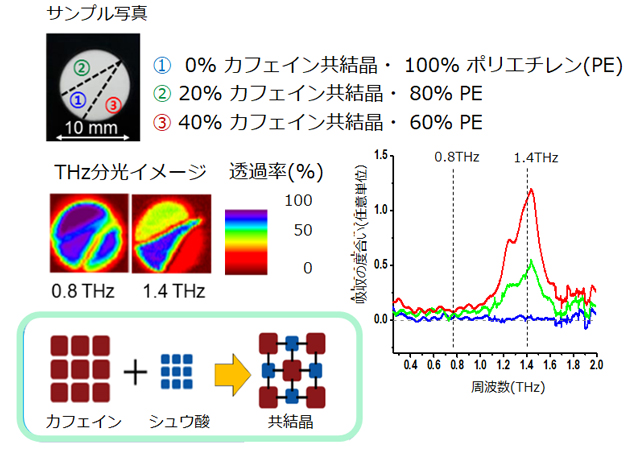
難水溶性のAPI結晶であっても、水に易溶性の高い添加剤結晶と共結晶化することによりその溶解性を飛躍的に高め、薬物の吸収性を向上できる。例えば、APIのカフェイン結晶は溶解性が低いが、溶解性の高いシュウ酸を加えて、カフェイン:シュウ酸の共結晶(ここではカフェイン共結晶とよぶことにする)を合成することによって溶解性が高くなる。共結晶にする前のカフェイン結晶やシュウ酸結晶それぞれにはTHz波の吸収がほとんどないが、水素結合など分子間相互作用が強く働くことによって共結晶には高いTHz吸収ピークが1.4THz付近にあることがTHzスペクトルから分かった[17]。図のテストサンプル錠剤の共結晶の濃度は左上が20%、右下が40%で、共結晶の吸収のない0.8 THzと共結晶の吸収のある1.4 THzに周波数を固定して2次元のスキャンを行っている。透過率の低い部分がカフェイン共結晶の多い部分に対応し、非破壊・非接触で共結晶の濃度の2次元分布を得られることが分かった。この2次元分布は、水への溶解性やそれに伴う薬効とも深く関係すると考えられる。THz-FDSは周波数を固定化できることが、THz-TDSと比べて測定時間において優位となる。
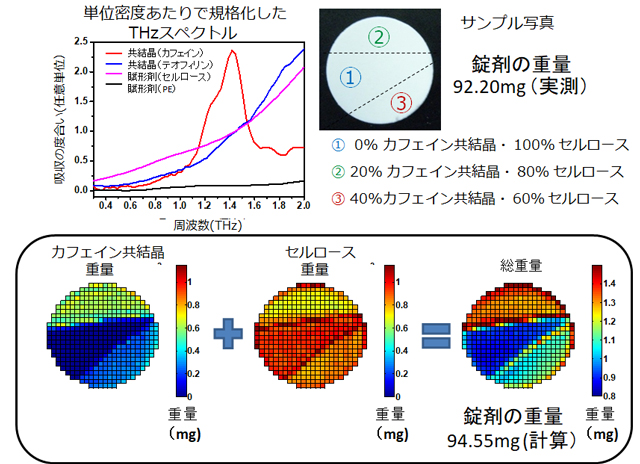
THz分光スペクトルのピークは医薬結晶などの固体サンプルでも比較的ブロードであったり、ピークが明確でない場合があるため、単純にピークの周波数をデータベース化するのでは定量分析をすることは難しいため、THzスペクトルを解析するためのデータサイエンスが必要となる。各成分のTHzスペクトルをデータベース化し、カーブフィッティングや主成分分析などの多変量解析を行うことで定量分析を行うことが可能となる。図8の例では、医薬品の共結晶として、カフェインとシュウ酸の共結晶とテオフィリンとシュウ酸の共結晶、錠剤を成型する賦形剤としてセルロースとポリエチレン、合わせ4本のTHzスペクトルを単位密度あたりで規格化してデータベース化した。この規格化によって、各成分の重量分布を知ることができる[18]。テスト錠剤は、3つの部分から成り、サンプル写真の中央付近は100%セルロース、上部は20%がカフェイン共結晶、下部は40%がカフェイン共結晶である。錠剤の重量は実測で92.20mgであった。図8のイメージはTHz分光から計算された、カフェイン共結晶とセルロースの各成分の重量分布である。単位密度あたりで規格化されたTHzスペクトルのデータベースから、計算することができる。前述したように、THz分光スペクトルのピーク比較的ブロードであったり、ピークが明確でない場合があるため、未だに高精度の定量分析は難しいのが現状である。カフェイン共結晶とセルロースの各成分の重量分布を加算することで、総重量のイメージとなる。このイメージの各ピクセルの重量を加えると、錠剤の重量の計算値が求められ、94.55mgとなった。実測の92.20mgと比較すると、約2.5%重くなっており、これが誤差といえる。分析化学の分野では、%オーダーの誤差は大きく、さらなる精度の向上が望まれる。
液体サンプルとして生体分子を含む水溶液では、図9にスペクトルの概念図を示すが、さらにピークがブロードとなり複雑化する。水分子だけでも、分子間伸縮振動、速い緩和、遅い緩和などのモードがあり、さらに、生体分子の水和(溶質の分子などが周囲の水分子と結合して1つの集団を形成すること)によるピークはTHz波領域よりさらに低い周波数帯のマイクロ波領域に存在する。そのため、マイクロ波分光と組み合わせることによって、THz波領域からマイクロ波領域までの、連続した広帯域のスペクトルを測定することができ、カーブフィッティングなどによって、スペクトル解析が可能となる[19]。これまでに、タンパク質の凍結や乾燥に対して生体分子保護機能を有するトレハロースにおいて, 濃度0.15モル/ℓでは第一水和層を上回る20個以上の水和水を有していることが分かった[20]。水和の状態は、ガンなどの細胞の変化に鋭敏であると考えられており、そのためにも今後さらなる水和状態の分子レベルでの解析が重要であるといえる。
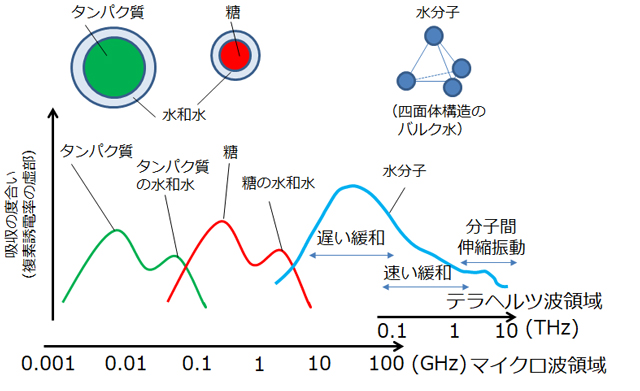
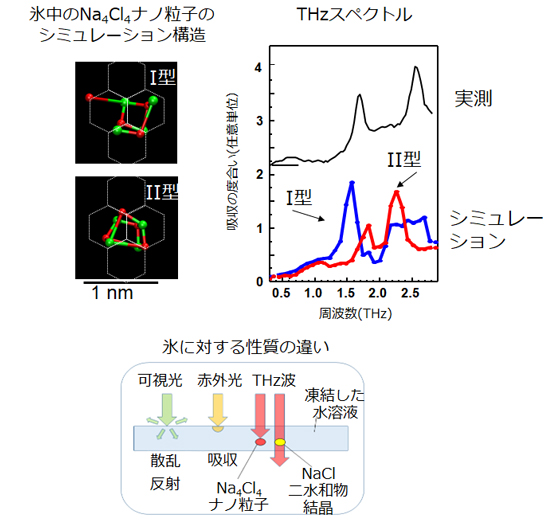
図10にフリーズドライ過程における塩化ナトリウムのナノ粒子であるNa4Cl4クラスタのTHzスペクトルを示す[21]。THz波は水の吸収が非常に高いが、氷に対しては透過する。純粋の氷は可視光が透過できるが、水に化学物質が溶解していると均一には凍結せず白濁し、可視光は散乱・反射するため透過できない。より長い波長の赤外光は吸収が大きく透過できないが、さらに波長の長いTHz波は透過する。そのため、フリーズドライ過程の様にこれまで把握することのできなかった凍結材料のプロセスモニターリングが可能となる。これまで、塩分(NaCl)は凍結の際に氷の結晶から排出されるか、あるいはNaCl・2H2Oという水和物になると考えられてきた。しかし、THzスペクトルには2つの明確なピークが見られ、NaCl やNaCl・2H2O には吸収がなかったため、分子動力学計算や非経験的分子軌道計算を用いたシミュレーションによって、Na4Cl4クラスタという約1nmの非常に小さなナノ結晶が2種類存在することを初めて発見した。フリーズドライは食品のみならず、ワクチンなど医薬分野でも利用されており、今後、医薬結晶のナノ結晶プロセス化学研究に役立つと期待できる。
このように、THzスペクトルの解析にはデータサイエンスが必要であり、これにより定性・定量分析、水和状態に基づくガン研究、ナノ結晶の研究が進むと思われる。
5.まとめ
本稿では、THz波センシング技術の基本原理、医薬分野を中心にIoTセンシングとしての優位性やデータサイエンスの活用の必要性などについて解説した。今後のTHz波IoTセンシングの高性能化・小型化とTHzデータサイエンスによるスペクトル解析技術の向上によって用途は飛躍的に広がり、安心・安全のための非破壊・非接触のセンシング技術として世の中に貢献することを期待したい。
謝辞
本報告をまとめるに際し、中村昌人氏、徐照男氏、瀬山倫子博士、児玉聡博士(NTT先端集積デバイス研究所),上野祐子博士(NTT 物性科学基礎研究所)に御協力を頂いたので深く感謝する。
参考文献
10) K. Ajito, Terahertz Spectroscopy Methods and Instrumentation, Chapter 18, Encyclopedia of Spectroscopy and Spectrometry 3rd Edition, pp.432-443, 2016.12, Academic Press, Elsevier.
11) H.-J. Song, K. Ajito, Y. Muramoto, A. Wakatsuki, T. Nagatsuma, IEEE Microwave and Wireless Components Letters, 22, 7(2012) 363-365 .
12) J.-Y. Kim; H.-J. Song, M. Yaita,; A. Hirata, K. Ajito, Optics Express, 22, 2(2014) 1735–1741.
13) M. van Exter, Ch. Fattinger, D. Grischkowsky, Optics Letters, 14, 20(1989) 1128-1130 .
14) 味戸克裕, 電子情報通信学会誌, ,97, 11(2014) 964-970.
15) S. S. Dhillon, M. S. Vitiello, E. H. Linfield, A. G .Davies, M. C. Hoffmann, J. Booske, C. Paoloni, M. Gensch, P. Weightman, G. P. Williams, Journal of Physics D: Applied Physics, 50, 4(2017) 043001.
16) J.-Y. Kim, H.-J. Song, M. Yaita, A. Hirata, and K. Ajito, Optics Express, 22, 6(2014)1735-1741.
17) D. M. Charron, K. Ajito, J.-Y. Kim, Y. Ueno, Analytical Chemistry, 85, 4(2013)1980−1984.
18) J.-Y. Kim, R. Boenawan, Y. Ueno, K. Ajito, Journal of Lightwave Technology, 32, 20(2014) 3768− 3773.
19) 白神慧一, Optronics, 38, 5 (2019) 84-88.; 中村昌人, 田島 卓郎, 瀬山倫子, 電子情報通信学会論文誌 C, J101–C, 6(2018) 258-265.
20) K. Shiraga, A. Adachi, M. Nakamura, K. Ajito, Ogawa, The Journal of Chemical Physics, 146 (2017)105102.
21) K. Ajito, Y. Ueno, J.-Y. Kim, T. Sumikama, Journal of the American Chemical Society, 140, 42(2018) 13793−13797.
【著者紹介】
味戸 克裕(あじと かつひろ)
日本電信電話株式会社 NTT先端集積デバイス研究所 主任研究員
■略歴
1995年 東京大学大学院工学系研究科応用化学専攻博士課程修了、同年日本電信電話(株)(NTT物性科学基礎研究所)入社。ミリ波・テラヘルツ光を使った分析化学および超高速無線技術、多孔質材料や光ピンセット技術を使った脳神経伝達物質のラマン分光分析法、医薬品のIoT非破壊イメージング検査技術などのセンサとデータサイエンスの研究に従事。
2010〜2014年 日本分光学会理事
2017〜2018年 千葉工業大学機械サイエンス学科非常勤講師
2018年 横浜国立大学理工学部数物・電子情報系非常勤講師、京都大学農学部森林科学科非常勤講師
2018年〜 電気学会センサ・マイクロマシン部門幹事(広報担当)
2018年~ 早稲田大学先進理工学部非常勤講師
IEEE学会会員、電子情報通信学会会員、アメリカ化学会会員、電気学会会員、日本分光学会会員、日本分析化学会会員
