
教授
吉信 達夫
1. はじめに
さまざまな分野において、試料中に含まれる特定の化学種(イオンや分子)の分布を観察・定量したいという需要があるが、そうした場合の第一選択肢は光学的な観察手法であるといえる。測定したい化学種が有色の場合はもちろん、そうでない場合も何らかの呈色反応や発光現象を利用することができれば標的化学種の濃度分布を可視化することができる。医学・生物学分野では古くから標本の染色が用いられ、さまざまな染色法や色素が開発されてきたが、さらに近年はデジタルカメラの性能向上により高解像度・高精細の画像や動画を高感度に得ることができ、顕微鏡や分光学的手法との組み合わせも容易である。
一方、何らかの制約から光学的な観察手法が適さない応用も存在する。生体試料における色素の毒性が問題となるケースはその一例である。また、試料に光を当てると反応してしまう場合や、空間的な制約から光学系を用いることができない場合もある。そのような場合に適用できるセンサ技術の1つとして、本稿では光走査型の半導体化学イメージセンサについて紹介する。
2. 半導体化学センサデバイス
2.1 ISFET
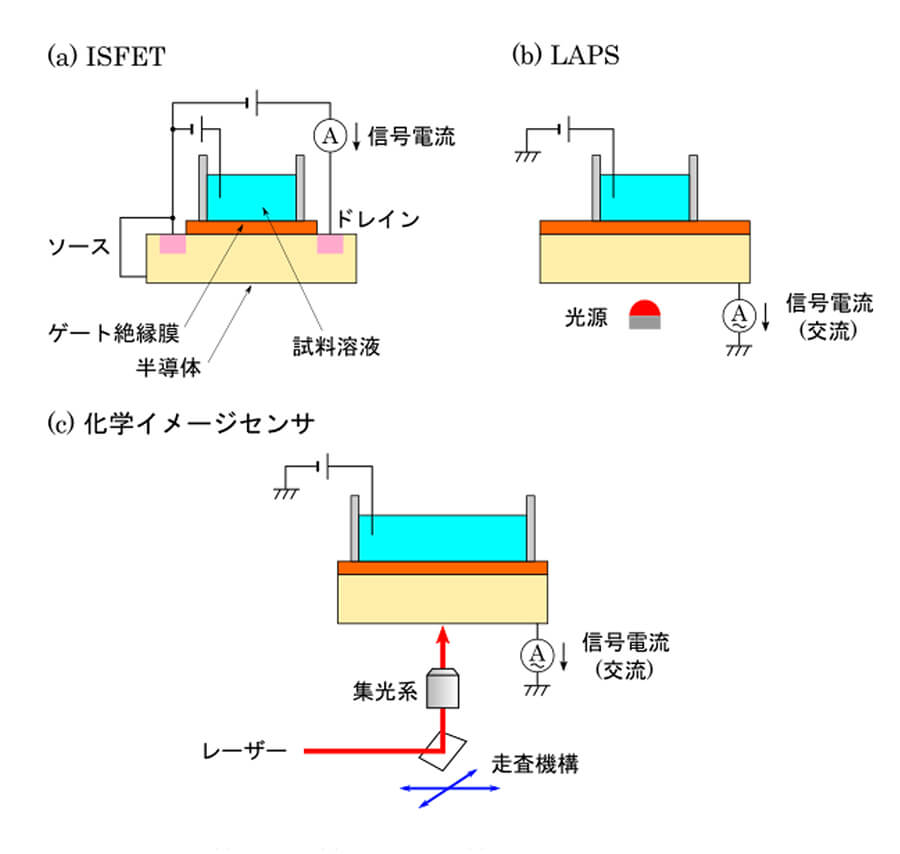
半導体デバイスを用いた化学センサとしては1970年にBergveldが提唱したイオン感応性電界効果トランジスター(Ion-sensitive field-effect transistor; ISFET)が実用的にも広く普及している[1]。ISFETは図1(a)のようにMOS型電界効果トランジスター(metal-oxide-semiconductor field-effect transistor; MOSFET)のメタルゲートを除去して絶縁膜表面が露出した構造を有し、これをセンサ面として試料溶液と直接接触させることにより、標的化学種の濃度に応じた電位差が表面に生じる。絶縁膜表面の電位に応じて半導体中の電荷分布が変化し、ソース-ドレイン電極間のコンダクタンスが増減することを利用して信号を読み出す。ポータブルなpHセンサとして市販されているほか、センサ面を感応膜で修飾することによってさまざまな化学種に対応した化学センサ・バイオセンサが開発されてきた。
2.2 LAPS
その後、1988年にHafemanらによって提唱されたのがLAPS (light-addressable potentiometric sensor) である。LAPSの場合も、標的化学種の濃度に応じて絶縁膜表面の電位が変化し、半導体中の電荷分布が変わるところまではISFETと同じであるが、それを読み出すために半導体を光照射して発生する光電流を用いる点が異なる。光はセンサ面の上方から(すなわち試料溶液を透過する形で)照射することもできるが、それとは反対側のセンサ裏面から照射することもでき、その場合、試料そのものには光が当たらない(図1(b))。
ISFETと比較した場合、LAPSは以下の特長を有する。(1)ISFETの測定領域はゲート領域に固定されるが、LAPSの測定領域は光を照射する範囲を変えることで自由に定義できる。そのため、1枚のセンサ上に多数の測定点を設けて複数の検体を測定したり、あるいは1枚のセンサ上に異種感応膜を集積して複数の化学種を標的とするマルチアナライトセンサを作製することが可能である。(2)ISFETを製造するためには、トランジスター構造を形成して配線する工程が必要であるが、LAPSは半導体基板上に絶縁膜を堆積しただけの単純な構造を有する。センサを消耗品として扱わなければならない応用(使用環境のためにセンサ面が劣化しやすい場合や、衛生管理上ディスポーザブル使用が不可欠な医療用途等)において、センサを安価に製造できることは大きな利点である。(3)シリコンウェハ全面を測定領域として用いることができるので大型試料に対応できる。
ISFETとLAPSは最終的な信号の読み出し方法が異なっているが、両者ともセンサ面上で標的化学種の濃度に応じた電位を発生させる機構は共通であるため、ISFETで使われてきた絶縁膜や感応膜の多くはLAPSにおいても利用可能である。LAPSのセンサ面上にイオノフォアを含む感応膜を作製することによってさまざまなイオン種の濃度測定が行われているほか、酵素反応や抗原-抗体反応、DNAのハイブリダイゼーション、アプタマーによる分子認識などバイオセンサへの応用も盛んに研究されている[3]。
2.3 化学イメージセンサ
上述のとおり、LAPSは1枚のセンサで多検体あるいは多項目の測定に対応可能な技術として考案されたものであるが、これを標的化学種の濃度分布の可視化に応用したものが本稿で紹介する光走査型化学イメージセンサである[4,5]。なお、これとは別に集積回路技術を用いてISFETをアレイ状に並べて配線したもの[6]やCCD技術を用いた化学イメージセンサデバイス[7]も開発されている。
光走査型化学イメージセンサシステムの典型的な構成の模式図を図1(c)に示す。レーザー光を1点に集光する光学系を備え、XYステージまたはミラースキャナでセンサ裏面を光走査する。光電流信号はセンサ裏面のオーミック電極から取り出し、トランスインピーダンスアンプで電圧信号に変換したのちAD変換を行ってPCに収録する。励起光は一定の周波数で変調されており、光電流信号に含まれる当該周波数成分をロックイン検出し、各画素位置での信号を記録して標的化学種の濃度分布画像を生成する。空間的な分解能は集光系の性能と半導体中におけるキャリアの拡散距離によって決まり、最も高い場合でサブミクロン程度である。
一方、時間的な分解能に関しては、走査型の手法であるため各画素データを逐次的に収集する場合、画素数に比例した時間を要するという問題がある。例えば1画素あたり10ミリ秒の測定であっても、128×128画素の測定には約3分の時間を要する。そこで考案されたのが周波数多重型の測定システムである。各画素位置をそれぞれ異なる周波数で変調された多数の光で同時に照明することにより、各周波数成分が重畳した光電流信号が得られ、これを各周波数成分に分解すれば全画素位置のデータを同時に取得できる。現在までに64チャネルの周波数多重化で毎秒200コマの動画記録あるいは毎秒30コマのリアルタイム画像生成が達成されている。
動画 リアルタイムpHイメージングのデモ動画
次回に続く-
参考文献
- Bergveld P. 1970. Development of an ion-sensitive solid-state device for neurophysiological measurements. IEEE Trans. Biomed. Eng. 17, 70-71.
- Hafeman DG, Parce JW, McConnell HM. 1988. Light-addressable potentiometric sensor for biochemical systems. Science 240, 1182-1185.
- Yoshinobu T, Schöning MJ. 2021. Light-addressable potentiometric sensors (LAPS) for cell monitoring and biosensing. Current Opinion in Electrochemistry 28, 100727.
- Nakao M, Yoshinobu T, Iwasaki H. 1994. Scanning-laser-beam semiconductor pH-imaging sensor. Sens. Actuators B 20, 119-123.
- Yoshinobu T, Miyamoto K, Werner CF, Poghossian A, Wagner T, Schöning MJ. 2017. Light-addressable potentiometric sensors for quantitative spatial imaging of chemical species. Annual Review of Analytical Chemistry 10, 225-246.
- Yeow TCW, Haskard MR, Mulcahy DE, Seo HI, Kwon DH. 1997. A very large integrated pH-ISFET sensor array chip compatible with standard CMOS processes. Sensors and Actuators B 44, 434-440.
- Sawada K, Mimura S, Tomita K, Nakanishi T, Tanabe H, Ishida M, Ando T. 1999. Novel CCD-based pH imaging sensor. IEEE Transactions on Electron Devices 46, 1846-1849.
【著者紹介】
吉信 達夫(よしのぶ たつお)
東北大学 大学院 医工学研究科 バイオセンシング医工学分野 教授
■略歴
- 1987年京都大学工学部電気工学第二学科卒業
- 1989年京都大学大学院工学研究科電気工学第二専攻修士課程修了
- 1992年京都大学大学院工学研究科電気工学第二専攻博士後期課程単位取得退学
- 1992年大阪大学産業科学研究所 助手
- 1992年京都大学 博士(工学)
- 1996年大阪大学産業科学研究所 講師
- 1999年ドイツ・ユーリッヒ研究センター薄膜イオン技術研究所 客員研究員
- 2001年大阪大学産業科学研究所 助教授
- 2005年東北大学大学院工学研究科電子工学専攻 教授
- 2008年東北大学大学院医工学研究科 教授
- 現在に至る
