
准教授
長峯 邦明
2.3 ハイドロゲルを利用した安静時汗採取・検出デバイス
そこで筆者らは、皮膚に水溶液を接触させるだけで簡便に安静時の汗成分を採取できるという、分析化学の分野で利用されてきた汗成分採取法に着目した 23)。本手法では、水溶液が汗腺内の汗と接触することで、汗成分が水溶液中に拡散して採取される。これまで筆者らは、本手法によりグルコース、乳酸、Na+イオン、K+イオン、Cl–イオン、NH4+イオン、IgGの定量に成功している 24)。また、定期的な汗成分の採取と定量を繰り返すことで、汗成分の日内変動を追跡可能であることも既に確認している。汗成分採取液には前記以外にも様々な物質が含まれると予想されるため、検出対象の選定により広く応用展開できるものと期待している。
筆者らは、汗成分採取液として用いたリン酸緩衝生理食塩水(Phosphate buffer saline、PBS)を固体化することで、本汗採取・検出のデバイス化を試みた 25)。具体的には、PBSを含むアガロースハイドロゲルを、酵素修飾電極表面に固定化した。ゲルに皮膚を接触させるだけで安静時の汗成分が採取され、そのまま酵素修飾電極で汗成分の検出を連続的に行える。これにより、必要な時にゲルに触れるだけでいつでも安静時汗成分を採取・検出できるという全く新しい計測法が創出された。この簡易なデバイス構成は、例えば既存のセンサを汗成分センサに改良することも可能にする。例えば、図1は市販の小型ナトリウムイオンセンサ(堀場社製、LAQUAtwin Na-11)であるが、その感応部表面にPBSを含ませたろ紙を貼付し、そのまま汗中Na+イオンセンサとして利用した 26)。つまり、PBS含浸ろ紙に指を触れるだけで汗が採取され、そこに含まれるNa+イオン濃度を定量できる。筆者らは、市販センサが存在する場合はそれを少し改良してすぐに応用に繋げ、特殊なバイオマーカーを検出対象とする場合はセンサ感応膜を独自に研究開発している。
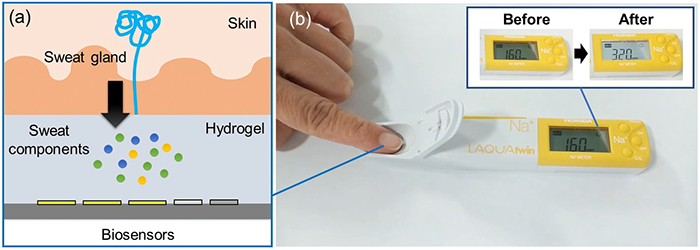
(b) 市販小型Na+イオンセンサを用いた汗成分採取・検出のデモ写真(参考文献25より引用。https://creativecommons.org/licenses/by/4.0/)。
同様の構成を有する安静時汗成分センサの研究開発がその後急速に進展し、乳酸 27,28)だけでなくグルコース 29,30)、Cl–イオン 31)、コルチゾール 32)、L-Dopa 32)、アルコールとアセトアミノフェン 34)、あるいはそれらのマルチセンシング 35,36)が実現されている。また、ハイドロゲルの種類も寒天だけではなく、柔軟・丈夫、かつ多孔質なポリビニルアルコールが使用され、体表に触れた時の圧力に対する耐性と、採取された汗成分の拡散を改善している。筆者らは本センサのウェアラブル化を目指し、山形大学大学院有機材料システム研究科の松井弘之 准教授と共に、アガロース被覆バイオセンサチップと自作小型回路基板(電気化学測定回路と無線通信素子を搭載)を組み合わせたウェアラブル汗成分センサを開発している(図2)。短時間であれば、体表への装着中にアガロースゲル内に採取・蓄積される汗成分を無線で連続モニタリングできる。得られたグラフの微分から、採取された汗成分濃度の変化速度を知ることもできる。
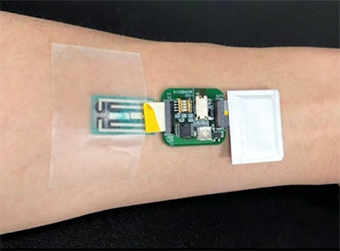
一方で、本手法ではゲル内での発汗量を定量する技術がほとんど無い。そのため、測定したシグナルの変化が汗成分濃度の変化に由来するのか、あるいは発汗量の変化に由来するのかを識別することが困難であり、測定結果の個人差を考慮することが難しい。そこで新たなデバイスとして、ウェアラブル微小流路デバイスとの組み合わせが検討されている。微小流路入口にハイドロゲル膜を設置し、ハイドロゲルで採取した汗を、その背面の微小流路内に導入することで発汗量を定量している 36)。あるいは、ハイドロゲルではなく、皮膚を底面とする微小流路を体表に設置し、流路内に(皮膚表面に)一定流速のPBSを流し続けることで汗中成分の連続定量可能なデバイスも報告されている 37,38)。以上、いずれも「面倒な発汗誘導を必要としない」ことをコンセプトとする新たな安静時汗成分センサであり、日常健康管理用デバイスとしての応用に向けて確実に進歩している。
3.まとめ
本稿では、非侵襲的な安静時汗成分計測へ向けた近年の研究開発動向に関して、特に、面倒な発汗誘導が不要な新規安静時汗成分センサを中心に紹介した。汗成分は他の外分泌性体液成分と比較して夾雑物の存在量が少なく、また、ハイドロゲル等を用いれば安静時の汗を非侵襲的にいつでも採取できるため、日常健康管理の指標としては有力な候補の1つと考えている。一方で上述のように、結果の個人差を考慮した測定の実現にはデバイス側の進歩は引き続き必要である。そして、汗成分と病気の関連性に関しては未だ医学的知見が乏しい。今後もセンサ開発と汗成分分析を同時に進めながら、汗成分センサがSociety5.0社会で目指す医療・ヘルスケアの実現に貢献しうるデバイスとなることを期待している。
参考文献
- T. Tsuda, S. Noda, S. Kitagawa, T. Morishita: Proposal of sampling process for collecting human sweat and determination of caffeine concentration in it by using GC/MS, Biomed. Chromatogr., 14, pp.505-510 (2000).
- K. Nagamine, A. Nomura, Y. Ichimura, R. Izawa, S. Sasaki, H. Furusawa, H. Matsui, S. Tokito, Printed organic transistor-based biosensors for non-invasive sweat analysis, Anal. Sci. 36(3), pp.291-302 (2020).
- K. Nagamine, T. Mano, A. Nomura, Y. Ichimura, R. Izawa, H. Furusawa, H. Matsui, D. Kumaki, and S. Tokito: Non-invasive sweat-lactate biosensor emplsoying a hydrogel-based touch pad, Sci. Rep. 9, pp.10102 (2019).
- K.Nagamine, Sens. Mater., 34(8), pp.3147-3154 (2022).
- S. Lin, B. Wang, Y. Zhao, R. Shih, X. Cheng, W. Yu, H. Hojaiji, H. Lin, C. Hoffman, D. Ly, J. Tan, Y. Chen, D. D. Carlo, C. Milla, and S. Emaminejad: Natural perspiration sampling and in situ electrochemical analysis with hydrogel micropatches for user-identifiable and wireless chemo/biosensing, ACS Sens. 5, pp.93-102 (2020).
- L. Yin, J. M. Moon, J. R. Sempionatto, M. Lin, M. Cao, A. Trifonov, F. Zhang, A. Lou, J.M. Jeong, S. J. Lee, S. Xu, J. Wang, A passive perspiration biofuel cell: high energy return on investment, Joule, 5, pp.1888-1904 (2021).
- J. R. Sempionatto, J. M. Moon, and J. Wang: Personalized data processing for predicting blood glucose concentrations, ACS Sens., 6, pp.1875-1883 (2021).
- P. H. Lin, S. C. Sheu, C. W. Chen, S. C. Huang, and B. R. Li: Wearable hydrogel patch with noninvasive, electrochemical glucose sensor for natural sweat detection, Talanta, 241, pp.123187 (2022).
- Y. Ichimura, T. Kuritsubo, K. Nagamine, A. Nomura, I. Shitanda, and S. Tokito: A fully screen-printed potentiometric chloride ion sensor employing a hydrogel-based touchpad for simple and non-invasive daily electrolyte analysis, Anal. Bioanal. Chem., 413, pp.1883-1891 (2021).
- W. Tang, L. Yin, J. R. Sempionatto, J. M. Moon, H. Teymourian, and J. Wang: Touch-based stressless cortisol sensing, Adv. Mater., 33, pp.2008465 (2021).
- J. M. Moon, H. Teymourian, E. De la Paz, J. R. Sempionatto, K. Mahato, T. Sonsa-Ard, N. Huang, K. Longardner, I. Litvan, and J. Wang: Non-invasive sweat-based tracking of L-Dopa pharmacokinetic profiles following an oral tablet administration, Angew. Chem. Int. Ed. Engl., 60, pp.19074-19078 (2021).
- S. Lin, J. Zhu, W. Yu, B. Wang, K. A. Sabet, Y. Zhao, X. Cheng, H. Hojaiji, H. Lin, J. Tan, C. Milla, R. W. Davis, S. Emaminejad, Proc. Natl. Acad. Sci. U. S. A., 119(15), pp.e2201937119 (2022).
- L. Wang, T. Xu, X. He, and X. Zhang: Flexible, self-healable, adhesive and wearable hydrogel patch for colorimetric sweat detection, J. Mater. Chem. C, 9, pp.14938-14945 (2021).
- H. Y. Y. Nyein, M. Bariya, B. Tran, C. H. Ahn, B. J. Brown, W. Ji, N. Davis, and A. Javey: A wearable patch for continuous analysis of thermoregulatory sweat at rest, Nat. Commun., 12, pp.1823 (2021).
- S. Konno, Y. Suzuki, M. Suzuki, H. Kudo, Evaluation of exercise intensity by real-time skin lactate monitoring system, Electron. Comm. Jpn., 103, pp.97-102 (2020).
- Y. Goto, Y. Suzuki, K. Morisawa, A. Hosoyama, Y. Taira, H. Kudo, Continuous assessment of sweat lactic acid secretion using microfluidic sweat lactic acid monitoring system, IOP Conf. Ser.: Mater. Sci. Eng., 1192, pp.012006 (2021).
【著者紹介】
長峯 邦明(ながみね くにあき)
山形大学 大学院 有機材料システム研究科 准教授
■略歴
2007年 東北大学大学院環境科学研究科博士後期課程修了(博士(学術))。同年より日立製作所中央研究所 研究員、東北大学大学院薬学研究科・理学研究科 COEフェロー、東北大学大学院工学研究科 助教を経て2017年1月より山形大学大学院有機材料システム研究科 准教授。同年から2021年まで文部科学省 卓越研究員を兼務。ヒトや植物、微生物などの生体情報のバイオセンシングの研究に従事。
