
医薬品等包装プロジェクト統括
樋口 泰彦
はじめに
「医薬品業界で求められる漏れ試験」とは、結論から述べると,「品質に影響を与える包装欠陥(形状)を検知し,その大きさ,度合いを計測する試験法」となる,以下にその詳細を解説する.
医薬品包装業界では,包装容器の完全性評価(密封性やガスバリア性評価)などの基準を見直す活動が進められており2021年6月に第十八改正日本薬局方(The Japanese Pharmacopeia 18th)(以降:JP181)に,関連する内容が告示された.ここでは「無菌医薬品の包装完全性評価」および「無菌医薬品包装の漏れ試験法」が参考情報として収載され医薬品包装品質に関する基準や試験法などの適正化に向けた活動が産官学一体となって進められている.
日本薬局方( Japanese Pharmacopoeia: JP)は,医薬品医療機器等法(薬機法)に基づき厚生労働大臣が定める医薬品の品質の適正化のための規格基準書である.生薬総則,製剤総則,一般試験法,医薬品各条(医薬品登録)などから構成されている.
本稿では,医薬業界の動向と現状・問題点を踏まえJP181)・USP<1207>2)(米国薬局方)の方向性を基にその対応策を解析理論,実施手順,試験法選定など総合的に「医薬業界が求める漏れ試験」について解説を行う.
1. 医薬業界の国内外の動向
医薬業界は国際的な幾つかの枠組みによりその方向性が示唆されている.
その中の一つが1990年に創設されたICH(International Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use)医薬品規制調和国際会議である.ここでは医薬品のグローバル化に対応し,安全で有効性の高い医薬品を確実に開発,流通する事を目指し各国規制当局および製薬企業が協働し世界的な規制調和活動を行っている.
もう一つの枠組みが,1970年に締結され1995年から各国医薬品査察当局が参加したPIC/S(医薬品査定協定・医薬品査察協同スキーム)がある.ここでは各国医薬品査察当局が参加し医薬品GMP(Good Manufacturing Practice:品質が保証された製造工程)に係る指針を作成,査察の国際整合を図るとともに,相互査察が進むよう活動を続けている.この様に,医薬品業界はレギュレーション(法規制)と査察(チェック体制)の両面で国際調和(ハーモナイゼーション)に向けた活動を世界規模で進められている.
昨年告示されたJP181)は,前年に公開されたUSP<1207>(米国薬局方2)をベースに構成されており完全性の評価基準や各種試験法はUSPを踏襲する形で作られている.
国際調和は、主に3地域(米国・ヨーロッパ・日本)の薬局方(3局)を対象に行われている.この3地域は新薬の開発,製造が主に行われている地域であり国際的に薬局方をリードしている.
2. 医薬品包装業界の現状
医薬品包装には大きく無菌医薬品包装(アンプル・バイアル・プレフィルドシリンジ:液剤が充填された瓶・注射器・輸液バッグ・パウチ)と経口剤包装(PTP・ピロー・三方シール・ボトル)など大きく2種類に分かれている.今回JP18に収載されたものは「無菌医薬品包装の完全性評価基準」であり,バイアルやプレフィルドシリンジなどの注射剤が対象となっている.求められる包装機能としては外部からの有害ガス(酸素・水蒸気・二酸化炭素)及び微生物,埃,塵,光などの侵入を防止する機能と包装内部からの製剤の漏洩防止,蒸散防止などがある.無菌製剤と経口剤では微生物に対するバリア機能を除けばほぼ同等と考えることが出来る.
表-1は注射剤容器(バイアル)に対する製薬企業での試験状況について2016年の日本PDAの調査データである.6年前のものであるが現在もほぼ同様の状況である.多く製薬企業で定性的漏れ試験を抜取検査で実施していることが分かる.また経口剤についても同等の結果が報告されている.
注)PDA(Parenteral Drug Association):医薬品および医療機器の開発,製造関する技術やGMPの分野で世界的に指導的立場にある国際的学術団体
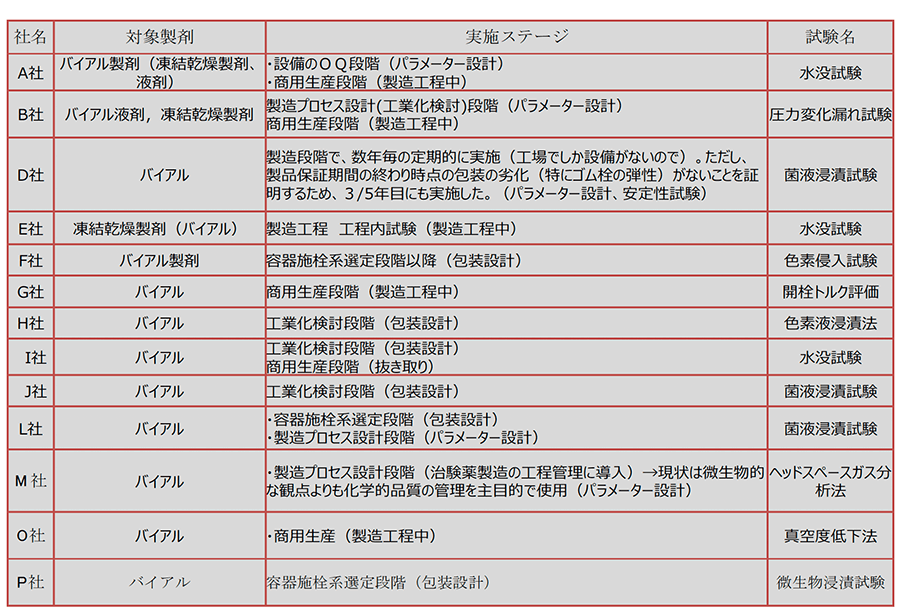
対象企業13社の内4社が定量的試験法を採用しているが,他の9社が定性的試験法を採用している事がわかる.表中の試験内容については詳細を10項「試験法選定」表-6~表-8にて解説する.
3. 現状の問題点と対処
- ● 問題点を整理すると以下のようになる.
- 3-1 現在、医薬包装の多くが水没試験,液体漏れ試験,微生物侵入試験などの定性的漏れ試験により品質が管理されている.定性的漏れ試験では測定条件により測定結果に大きなバラツキが生じ結果に対する科学的妥当性や評価基準の根拠が不明確である.(液没試験や液体漏れ試験とガスバリア性能,微生物汚染特性との相関性が不明確である)
- 3-2 安定性試験(医薬品の一部ロットに対し経時的に品質確認を行う試験)結果が完全性評価妥当性の根拠となっている.(プロセスでは無く結果で評価している)
- 3-3 医薬品包装の完全性評価基準が明確に規定されていないため「漏れなきこと」が実質的な基準となり水没試験,液体漏れ試験などが適用されている.しかし,現状の包装素材においては漏れの無いものは存在せず気体の透過やピンホールは確実に存在いている.(漏れの無き事は現実的ではない)
- 3-4 医薬品包装の完全性評価に適した定量的漏れ試験法の開発,導入が遅れている.
- 3-5 包装完全性の判定基準に対する考え方,手順,理論が確立されていない.
- 3-6 安定性試験に用いるサンプルに完全性に問題があるものが混在した場合,試験結果の信頼性が失われる可能性がある.(安定性試験で問題が生じた場合,対象ロットは回収となり莫大な損失が生ずる)
- 3-7 水没試験が破壊試験であるため,抜取検査のサンプルは問題が無いものまで全て廃棄されている.(医薬品ロスにつながっている)
- ● 対処
-
3-8
対処の方向性
以上の問題点から対処すべき課題として以下の方向性を導き出すことが出来る.
「医薬品に対する要求品質に適合した包装容器完全性評価基準を確立し,基準を満たすための科学的根拠を有する手順,理論,試験法」が求められている.
JP18・USP<1207>の示す方向性を基に,これら問題にどの様に対処すべきかを解説する.
4. JP18およびUSP<1207>の方向性
JP18はUSP<1207>をベースに構成されたため主要な項目で同一の方向性を示しており相違点は一部である.
「表-2 JP18・USP<1207>対比表」に用語の定義を示し,右端の欄に同一度合いを現す記号(〇,◎,×)を表記した.
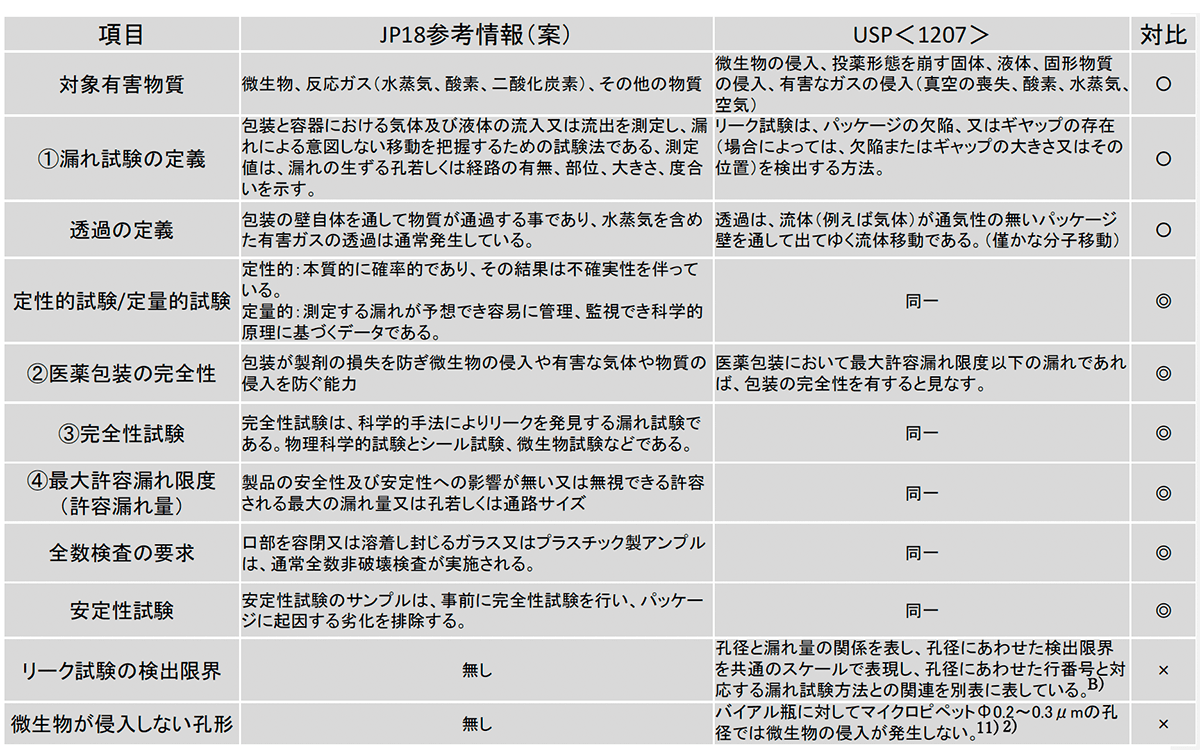
注目すべきは①から④ の定義であり漏れ試験の考え方に欠陥形状の要素を取り入れ,科学的根拠を持った評価基準を示している.特に②医薬包装の完全性 ④最大許容漏れ限度の定義はリスクマネージメントをベースとした考え方である事が分かる.(製剤品質を基準とした考え方)
5. 注目すべき4つの考え方(方向性)
5-1「漏れ試験の定義」について
従来の考え方は,「気体及び液体の流入又は流出を測定し,漏れによる意図しない物質移動を把握するための試験法であった.」これは,漏れ量を把握する事が漏れ試験の目的である事を示している.しかしここでは,新たに「測定値は,漏れの生ずる孔若しくは経路の有無、部位,大きさ,度合いを示す.」が加えられている.つまり,漏れ量を測定する事でだけでは無く,孔の形や大きさ,度合いを示すものとしている.この考え方は,従来の漏れ試験には無かった新たな考え方である,この考え方が後に,完全性試験の本質的な問題(孔形状の定量化)を提起する事となる.
5-2「完全性試験の定義」について
JPTI2021(日本薬局方 技術情報2021)において,完全性試験とは医薬包装の欠陥を検知,検出する試験法を云い,漏れ試験・その他の品質試験・微生物試験に分類される.


注)JPTI2021(日本薬局方 技術情報):JP18改定部分の技術解説書,JPと同時に刊行される.
5-3「最大許容漏れ限度の定義」
「製品の安全性及び安定性への影響が無い又は無視できる許容される最大の漏れ量又は孔若しくは通路サイズ」これは,どの程度の欠陥又は孔であれば品質リスクが低いか若しくは無いかを科学的に証明することを求めている.これはリスクマネージメントの考え方であり,欠陥形状の定量化を求める根拠ともなっている.
5-4「医薬包装の完全性の定義」
「医薬包装において最大許容漏れ限度以下であれば包装の完全性を有するものと見なす.」
最大許容漏れ限度の定義より医薬品に対するリスクが無い又は低い欠陥形状最大値以下の孔若しくは欠陥であれば完全性を有する.つまり包装機能が良い状態であるとの判断基準を示している.これは「漏れ無き事」の科学的根拠を示している事となる.
次回に続く-
参考文献
- 第十八改正薬局方 (令和3年6月7日厚生労働省告第220号)
無菌医薬品の包装完全性評価(G7-4-180), 無菌医薬品の包装も漏れ試験法(G7-5-180) - USPharmacopeia,40(2017),〈1207.1〉PACKAGE INTEGRITY TESTING IN THE PRODUCT LIFE CYCLE _TEST METHOD SELECTION AND VALIDATION,<1207.2>PACKAGE INTEGRITY TEST TECHNOLOGIES
- 2019年日本表面真空学会学術講演会 吉田 肇、新井健太、武井良憲
「気体流れの全領域に適用可能な任意長さの円筒導管を通過する気体流量の簡易計算方法」 - 2019年日本真空学会学術講演会 北條 勤、猪股 順、原 努、平田真央
「孔を拡散により通過する気体の解析」 - 日本工業規格JISZ2329:2002「発泡漏れ試験方法」
- 日本工業規格JISZ2330:2012「非破壊試験法-漏れ試験方法の種類及びその選択」
- 日本工業規格JISZ2331:2006「ヘリウム漏れ試験法」
- 日本工業規格JISZ2332:2012「圧力変化による漏れ試験方法」
- ASTM F2338-09 Standard Test Method for Nondestructive Detection of Leaks in Packages
by Vacuum Decay Method (Reapproved 2013) - 山中 明:高電圧式ピンホール検査機 JPI Journal Vol.46 No.10,2008
- Kirsch LE,Nguyen L,Moeckly CS, Gerth R,Pharmaceutical container/closure integrity,
Ⅱ:The relationship between microbial ingress and Helium leak rates in rubber-stoppered glass vials, PDA Journal of pharmaceutical science & technology Vol 51,No5/September-October 1997.
【著者紹介】
樋口 泰彦(ひぐち やすひこ)
株式会社 フクダ 取締役 医薬品包装等プロジェクト統括
■略歴
- 1977年同社入社、国内営業、海外営業,営業企画など担当,2000年電子部品業界参入,2018年MUH-0100(世界最高レベルのヘリウム漏れ試験装置 10-15Pam3/s)同業界に発表.
- 医薬品業界において2016年 PMDA主管,日本薬局方原案審議委員会「無菌医薬品包装の完全性評価WG」に参画,第18改正薬局方 参考情報執筆.同年,日本薬局方技術情報(JPTI2021)執筆.
- 日本PDA製薬学会,ISPE日本本部,創包工学研究会,などの医薬包装関連委員会に参画,各種医薬包装関連セミナー実施.
- 2022年 孔形状規格化推進のため日本計量機器工業連合会・規格検討会参画.
